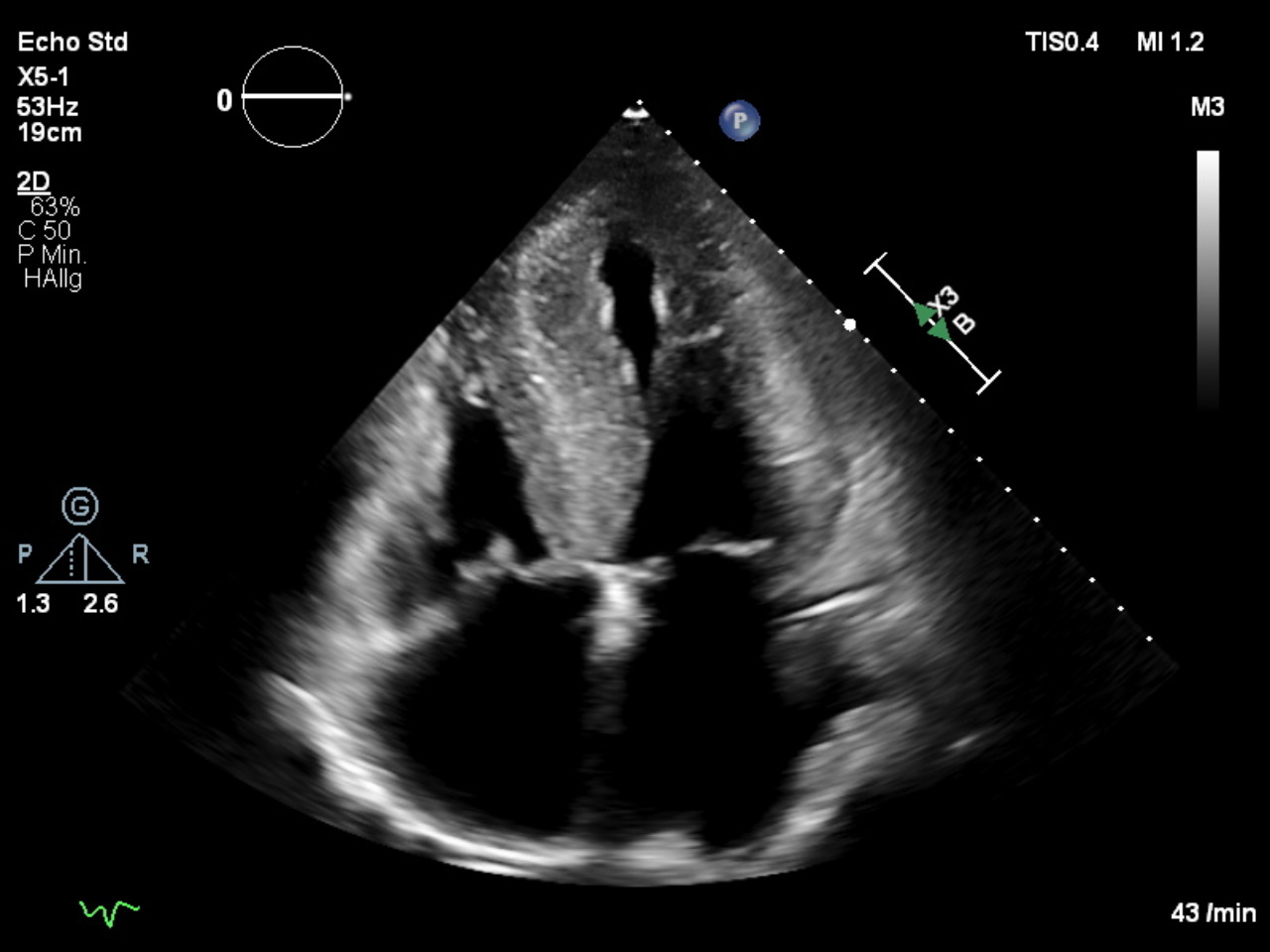
Kardiomyopathien
Team

PD Dr. med.
Lars Michel
Leitungsteam

Dr. med.
Florian Bühning

Dr. med.
Fabrice Reyes

Dr. med.
Stephan Settelmeier

Dr. med.
Julia Kirsten Vogel

Dr. med.
Loubna Yahsaly

Cand. med.
Sophia Jura
Doktorandin

Cand. med.
Farida Mahmudi
Doktorandin

Cand. med.
Svenja Roß
Doktorandin

Verena Schierhoff
Doktorandin

Katharina Soldat
Doktorandin

Hanna Pörtner
Doktorandin
Kardiale Amyloidose
Die kardiale Amyloidose wird durch Ablagerung von fehlgefalteten extrazellulären Proteinen (Amyloid-Fibrillen) im Herzen verursacht. Durch eine progrediente myokardiale Hypertrophie mit diastolischer Dysfunktion entwickelt sich eine Herzinsuffizienz mit hoher Relevanz für Morbidität und Mortalität betroffener Patient*innen. Obgleich die Erkrankung lange als Rarität betrachtet und durch unzureichende diagnostische Aufarbeitung oft übersehen wurde, haben die letzten Jahre gezeigt, dass es eine der häufigsten Herzmuskelerkrankungen ist und eher als Volkskrankheit des höheren Lebensalters bezeichnet werden muss.
Das Ziel des Schwerpunktes „Kardiale Amyloidose“ ist eine systematische Erfassung diagnostischer Maßnahmen, funktioneller und echokardiographischer Parameter, kardialer Biomarker sowie prognostischer Implikationen. Durch innovative wissenschaftliche Ansätze soll das Verständnis der kardialen Amyloidose, und damit die Behandlung betroffener Patient*innen verbessert werden. Einzelne hochinnovative Projekte beziehen sich auf Risikofaktoren, Versorgungsstruktur und zielgerichtete Diagnostik. Wissenschaftliche Ansätze basieren auf umfangreichen retro- und prospektiven Datenbanken, Analysen von Biobankproben und translationalen/grundlagenwissenschaftlichen Ansätzen.
Das Essen Amyloidosis Registry (EAR) (PD Dr. med. Lars Michel) bietet eine vollumfängliche retrospektive und prospektive Erfassung von Patient*innen mit Amyloidose. Das Ziel des Registers ist eine systematische Erfassung diagnostischer Maßnahmen, funktioneller und echokardiographischer Parameter, kardialer Biomarker sowie prognostischer Implikationen. Durch innovative wissenschaftliche Ansätze soll auf Basis von einzelnen Projekten und wissenschaftlicher Vernetzung das Verständnis der kardialen Amyloidose, und damit die Behandlung betroffener Patient*innen, verbessert werden.
Hypertrophe Kardiomyopathie
Die Hypertrophe Kardiomyopathie (HCM) ist eine genetisch bedingte Herzmuskelerkrankung, die durch eine ausgeprägte Verdickung des Herzmuskels charakterisiert ist. Die Folgen sind facettenreich und umfassen eine diastolische Dysfunktion, Herzinsuffizienz sowie lebensbedrohliche Herzrhythmusstörungen. Bei einem Großteil der betroffenen Patient*innen besteht zudem eine Verengung des Ausflusstrakts der linken Herzkammer (HOCM). Lange Zeit beschränkte sich die Therapie der HCM auf eine medikamentöse Basistherapie, interventionelle und operative Verfahren sowie bei entsprechendem Risikoprofil die Implantation eines Defibrillators. Seit dem letzten Jahr steht nun zudem ein zielgerichteter Myosin-Inhibitor zur medikamentösen Therapie zur Verfügung.
Das Ziel des Schwerpunktes „Hypertrophe Kardiomyopathie“ ist die systematische Erfassung diagnostische Verfahren, funktioneller und echokardiographischer Parameter, kardialer Biomarker sowie prognostische Aspekte, um somit ein verbessertes Krankheitsverständnis zu erreichen. Wir versuchen eine Verlaufsbeurteilung des Therapieansprechens unter Medikamentengabe durch Biomarker und elektrokardiographische Marker zu erreichen, stets mit dem Ziel, die Therapieergebnisse für betroffene Patient*innen langfristig zu verbessern.
Die Klinik für Kardiologie und Angiologie ist Teil des multizentrischen REDUCE Registers (Registry for patients with diagnosed hypertrophic obstructive Cardiomyopathy under Myosin-Inhibitor Therapy). Als Teil eines Netzwerks führender Zentren in der Diagnostik und Behandlung der Hypertrophen Kardiomyopathie leisten wir einen entscheidenden Anteil für den wissenschaftlichen Fortschritt auf dem Gebiet, um die Behandlung betroffener Patient*innen schnell und nachhaltig zu verbessern.
Aktuelle Projekte (engl.)
- Right ventricular dysfunction in patients with left ventricular assist device (F. Mahmudi, T. Lerchner)
- Delay in time to diagnosis in ATTR-cardiomyopathy- a real world data analysis (Dr. med. J. Vogel, S. Jura)
- Cardiac biomarkers for the monitoring of amyloid cardiomyopathy (S. Jura)
- Naturally occurring antibodies in diagnosis and prognosis of ATTR cardiomyopathy (Dr. med. S. Settelmeier)
- Characterization of myocardial DPD binding characteristics and interference with transthyretin stabilizers (Dr. med. S. Settelmeier)
- Assessment of proteomics in patients with wild-type ATTR cardiomyopathy: A two-phase exploratory analysis (Dr. med. J. Vogel, S. Jura, Dr. med. S. Settelmeier)
- Feasibility and safety of interventional edge-to-edge repair in patients with cardiac amyloidosis (Dr. med. J. Vogel)
- Right ventricular endomyocardial biopsy for the assessment of cardiomyopathies: A monocentric safety and feasibility analysis (S. Roß, T. Lerchner)
- Cardiac biomarkers for the monitoring of response to mavacamten in hypertrophic obstructive cardiomyopathy (Dr. med. F. Bühning)
- ECG hypertrophy markers for the assessment of response to mavacamten in hypertrophic obstructive cardiomyopathy (Dr. med. F. Bühning, H. Pörtner)
- Echocardiographic Remodeling in Hypertrophic Obstructive Cardiomyopathy During Myosin Inhibitor Therapy (J. Werner, Dr. med. F. Bühning)
Finanzierung
UMEA Junior Clinician Scientist Stipendium 2025: Dr. med. F. Bühning, Dr. med. T. Lerchner, Dr. med. F. Reyes, Dr. med. J. Vogel
UMEA Start-Up Grant: Dr. med. S. Settelmeier
Preise
Young Investigator Award der Deutschen Gesellschaft für Amyloid-Krankheiten (DGAK): Dr. med. S. Settelmeier
Förderpreis der Hans und Gertie Fischer Stiftung 2022: Dr. med. L. Michel
Präsentation als „Best of Congress“, Deutsche Gesellschaft für Kardiologie 2022: Dr. med. L. Michel
Best Paper Award, Medizinische Fakultät, Universität Duisburg- Essen 2019: Dr. med. L. Michel
ESC Congress Educational Grant, Europäische Gesellschaft für Kardiologie 2019: Dr. med. L. Michel
Posterpreis, Deutsche Gesellschaft für Kardiologie 2019: Dr. med. L. Michel
Präsentation als „Best of Congress – Translational Science”, Deutsche Gesellschaft für Hämatologie und medizinische Onkologie 2014: Dr. med. L. Michel
Posterpreis, Medizinische Fakultät, Universität Duisburg-Essen 2014: Dr. med. L. Michel
Young Investigators‘ Award, Deutsche Gesellschaft für Hämatologie und medizinische Onkologie 2013: Dr. med. L. Michel
Abstract Achievement Award, Amerikanische Gesellschaft für Hämatologie 2013: Dr. med. L. Michel
Aktuelle Publikationen
Fünf relevante Publikationen
Lerchner T, Mincu RI, Bühning F, Vogel J, Klingel K, Meetschen M, Schlosser T, Haubold J, Umutlu L, Dobrev D, Totzeck M, Rassaf T, Michel L. Cardiac magnetic resonance imaging in patients with suspected myocarditis from immune checkpoint inhibitor therapy – A real-world observational study. Int J Cardiol Heart Vasc. 2024 Dec 19;56:101581.
Vogel J, Jura S, Settelmeier S, Buehning F, Lerchner T, Carpinteiro A, Rassaf T, Michel L. Delays in diagnosis and treatment of ATTR cardiac amyloidosis: A real-world data analysis. ESC Heart Fail. 2025 Apr 28.
Vogel J, Lüdike P, Mahabadi AA, Rassaf T, Michel L. Dual transcatheter edge-to-edge repair in a patient with cardiac amyloidosis and severe secondary mitral and tricuspid regurgitation – A case report. Eur Heart J Case Rep. 2024. In press.
Settelmeier S, Kessler L, Varasteh Z, Mahabadi AA, Michel L, Papathanasiou M, Laschinsky C, Rischpler C, Fendler WP, Schlosser T, Umutlu L, Herrmann K, Rassaf T, Kersting D. FAPI PET Imaging Supports Clinical Decision Making in Academic Cardiology Practice: A Pictorial Imaging Vignette. JACC Cardiovasc Imaging. 2024 Jul;17(7):811-823.
Vogel J, Jura S, Settelmeier S, Lerchner T, Bühning F, Carpinteiro A, Rassaf T, Michel L. Biomarkers for monitoring patients with cardiac amyloidosis during transthyretin-stabilizer therapy. ESC Annual Congress 2024.